Methoden

Da Nervenzellen und einige andere Zellen elektrische Eigenschaften besitzen, ist es möglich mit elektrophysiologischen Techniken die elektrische Reaktion einzelner Zellen auf beispielsweise pharmakologische, oder optogenetische Manipulation zu untersuchen. Beispielsweise lassen sich Ströme, die durch Kanäle fließen oder auch Spannungsänderungen an der Membran einer Zelle messen. Unsere Arbeitsgruppe verwendet vor allem die Patch-Clamp-Technik, um die elektrischen Eigenschaften von erregbaren Zellen in Kultur und von Nervenzellen in akuten Hirnschnitten, unter Einfluss des Neurotransmitters Serotonin, zu untersuchen. Dies geschieht einerseits durch das Einwaschen von spezifischen Liganden, andererseits durch optogenetische Aktivierung von lichtaktivierbaren Serotoninrezeptorchimären.

Störungen im Serotoninhaushalt können eine Ursache für verschiedene Erkrankungen, wie Angst und Depressionen sein. Speziell die 5-HT1 Autorezeptoren, serotonerge G-Protein gekoppelte Rezeptoren (GPCRs), welche die Ausschüttung von Serotonin (5-HT) regulieren, sind für den Serotoninhaushalt entscheidend. Diese Autoregulation des serotonergen Systems interessiert uns besonders, da vermutlich Veränderungen innerhalb dieser Signalkaskaden für unterschiedlichste psychiatrische Erkrankungen verantwortlich sind.
Interessanterweise gibt es diese GPCRs auch auf nicht serotonergen Neuronen (Heteroregulation) des zentralen Nervensystems (ZNS), wo ihre Aktivierung verschiedene Auswirkungen haben kann. Es ist jedoch unklar, in welchem Maße auch die Heterorezeptoren Einfluss auf Angsterkrankungen und Depressionen nehmen. Bislang konnten diese intrazellulären Signalwege nicht gezielt untersucht werden, da die Möglichkeit fehlte, sie mit hoher zeitlicher und räumlicher Kinetik anzuschalten. Abhilfe schafft hier eine neue Methode der Optogenetik.
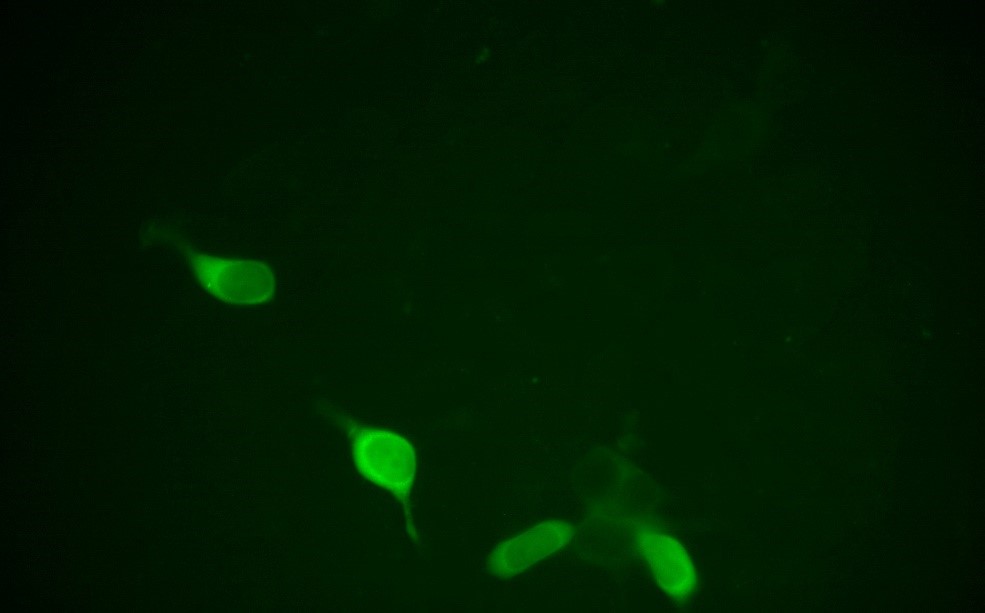
Calcium Imaging ist eine Methode, mit der die Aktivität von Neuronen, in vivo im Gehirn bei verschiedensten Verhaltenstests untersucht und sichtbar gemacht werden kann. Aktivierte Neuronen weisen eine Erhöhung der inneren Calciumkonzentration auf. Um diese sichtbar zu machen, werden auf dem grün fluoreszierenden Protein (GFP) basierte Calciumindikatoren (GECIs) über Virussysteme in das zentrale Nervensystem eingebracht. Die am gängigsten genutzten GECIs sind die so genannten GCaMPs, welche wir auch in unserem Labor verwenden. Mit Hilfe von Miniatur-Mikroskopen kann dann das Fluoreszenz Signal aufgenommen und analysiert werden.

Um Erkrankungen, die das Nervensystem betreffen, ausreichend untersuchen zu können sind Verhaltensversuche am lebenden Tiermodell unumgänglich. Je nach Forschungsschwerpunkt werden spezifische Verhaltensversuche durchgeführt, die optogenetisch manipuliert werden.
Mithilfe verschiedener Cre-Mauslinien lassen sich spezifisch bestimmte Zelltypen manipulieren, beispielsweise nur serotonerge Zellen. Unsere Versuchstiere werden gemäß des Tierschutzgesetzes und der Tierversuchsverordnung artgerecht gehalten. Es werden regelmäßige Gesundheitsuntersuchungen durchgeführt Ein Beispiel eines Verhaltensversuches, ist der Elevated-Plus-Maze-Test (EMP), bei dem die Ausprägung von Angst im Tier ermittelt wird. Die Arena besteht aus vier erhöht stehenden Armen, die zusammen ein Plus bilden. Zwei der Arme sind offen, die beiden anderen durch eine hohe Wand geschlossen. Im EPM steht das Versuchstier in Konflikt mit der Angst vor Höhe und dem Impuls neue Umgebung zu erkunden. Ein Maß für Angst ist hier die Zeit, die das Tier auf den offenen Armen verbringt, wobei eine längere Aufenthaltsdauer auf den offenen Armen ein Indikator für weniger Angst ist.
